#MONDE_TEST_COVIC19: Bamlanivimab, premier médicament autorisé par les Etats-Unis contre le Covid-19
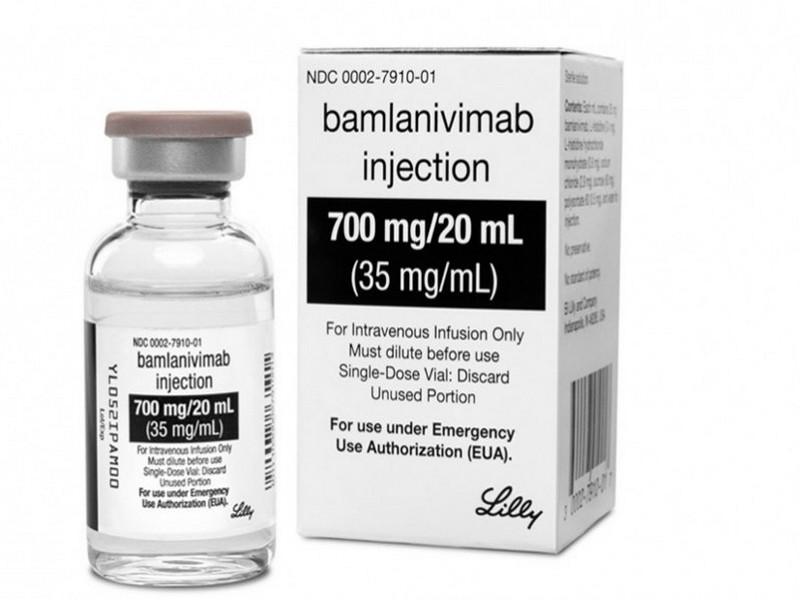
La Food and Drug Administration des Etats-Unis a délivré, le 9 novembre, une autorisation d'utilisation d'urgence (EUA) pour le traitement expérimental par anticorps monoclonaux Bamlanivimab pour le traitement du Covid-19 léger à modéré, chez les patients adultes et pédiatriques.
Le Food and Drug Administration des Etats-Unis est autorisé chez les patients ayant obtenu des résultats positifs au test viral direct du Sars-CoV-2, âgés de 12 ans et plus, pesant au moins 40 kilogrammes et présentant un risque élevé d'évolution vers un Covid-19 sévère et/ou hospitalisation. Cela comprend les personnes âgées de 65 ans ou plus ou qui souffrent de certaines maladies chroniques, explique la FDA, l'agence du département américain de la Santé et des services sociaux.
"Bien que l'innocuité et l'efficacité de ce traitement expérimental continuent d'être évaluées, il a été démontré dans les essais cliniques que le Bamlanivimab réduit les hospitalisations ou les visites à l'urgence liées au Covid-19 chez les patients à haut risque de progression de la maladie dans les 28 jours suivant le traitement par rapport au placebo", ajoute la même source.
Le Bamlanivimab n'est pas autorisé chez les patients hospitalisés en raison du Covid-19 ou nécessitant une oxygénothérapie: un effet du traitement par Bamlanivimab n'a pas été démontré chez ces patients. Les anticorps monoclonaux, tels que le Bamlanivimab, peuvent être associés à de pires résultats cliniques lorsqu'ils sont administrés à des patients hospitalisés nécessitant de l'oxygène à haut débit ou une ventilation mécanique.
"Les anticorps monoclonaux sont des protéines de laboratoire qui imitent la capacité du système immunitaire à lutter contre les antigènes nocifs tels que les virus. Ce médicament est un anticorps monoclonal spécifiquement dirigé contre la protéine de pointe du Sars-CoV-2, conçu pour bloquer l'attachement du virus et son entrée dans les cellules humaines."
"L'autorisation d'urgence du Bamlanivimab par la FDA fournit aux professionnels de la santé en première ligne de cette pandémie un autre outil potentiel dans le traitement des patients atteints de Covid-19", a déclaré Patrizia Cavazzoni, directrice par intérim du Center for Drug Evaluation and Research de la FDA. "Nous continuerons d'évaluer les nouvelles données sur l'innocuité et l'efficacité du Bamlanivimab dès qu'elles seront disponibles."
Les données étayant cette EUA pour le Bamlanivimab sont basées sur une analyse intermédiaire d'un essai clinique de phase 2 chez 465 adultes non hospitalisés présentant des symptômes légers à modérés du Covid-19. Parmi ces patients, 101 ont reçu une dose de 700 milligrammes de Bamlanivimab, 107 ont reçu une dose de 2.800 milligrammes, 101 ont reçu une dose de 7.000 milligrammes et 156 ont reçu un placebo dans les trois jours suivant l'obtention de l'échantillon clinique pour le premier Sars-CoV- positif.
L'EUA permet au Bamlanivimab d'être distribué et administré en une seule dose par voie intraveineuse par les prestataires de soins de santé.
Les effets secondaires possibles du médicament comprennent anaphylaxie et réactions liées à la perfusion, nausées, diarrhée, étourdissements, maux de tête, démangeaisons et vomissements.
Le 10 novembre 2020
SOURCE WEB PAR Médias 24
Les tags en relation
Les articles en relation

Mouhsine Lakhdissi rend le masque intelligent
Passionné de sciences, féru de poésie et amoureux de la nature, le coordinateur du projet MIDAD finalise avec son équipe son « masque intelligent de détec...

Maroc : très en colère, Mohammed VI sanctionne lourdement Casablanca
Le roi du Maroc, Mohammed VI, très en colère contre la situation qui prévaut dans son pays, principalement le comportement des populations de Casablanca, a i...

Youssef Amrani : SM le Roi a jeté les bases d’une véritable solidarité africaine
SM le Roi Mohammed VI a jeté les bases d’une véritable solidarité africaine en lançant une initiative commune de gestion des effets de la pandémie du nou...

Société Générale se met au service de ses clients en ces temps de crise
Parce que s’éloigner des autres en ces temps de crise est la manière la plus sûre pour se protéger contre le Covid-19, Société Générale s’adapte aux...
Coronavirus: plus de 40.000 morts dans le monde, près des trois quarts en Europe
La pandémie de nouveau coronavirus a fait plus de 40.000 morts dans le monde, dont près des trois quarts en Europe, depuis son apparition en décembre en Chin...
#MAROC_Vaccin_anti_Covid_DROITS_DES_CITOYENS: Voici les droits de citoyennes victimes d'effets indé
La responsabilité de l'Etat peut être invoquée avec ou sans faute. Mais prouver l'implication du vaccin dans la survenance d'effets secondaires g...

Coronavirus/Maroc: Tarfaya dépasse toutes les autres régions en termes de contaminations
La région de Laayoune Sakia El Hamra a enregistré un pic de contamination ces dernières 24 heures avec 37 cas ayant surgi à Tarfaya. Dans son bilan quoti...

MAROC_CORONA_RESTRICTIONS: DEUX SEMAINES DE PLUS A PARTIR DU 15 mars : Prolongation de deux semaines
Ce lundi 15 mars, le gouvernement a annoncé la prorogation de mesures restrictives de deux semaines, à compter du mardi 16 mars à 21h. Cette décision concer...

#MAROC_COVID19_Pr_Zouhair: Zoom - Covid-19 -La pandémie entame sa phase de régression-
Plus le virus se réplique, plus il s’affaiblit Une nouvelle vague au Maroc est peu probable! Saïd Zouhair, chef du laboratoire de bactériologie-v...

Covid-19: Comment RAM et ONDA maintiennent la flotte au sol
Sur le tarmac de l’aéroport international Mohammed V à Casablanca, une soixantaine d’appareils de types différents sont aujourd’hui cloués au sol. ...
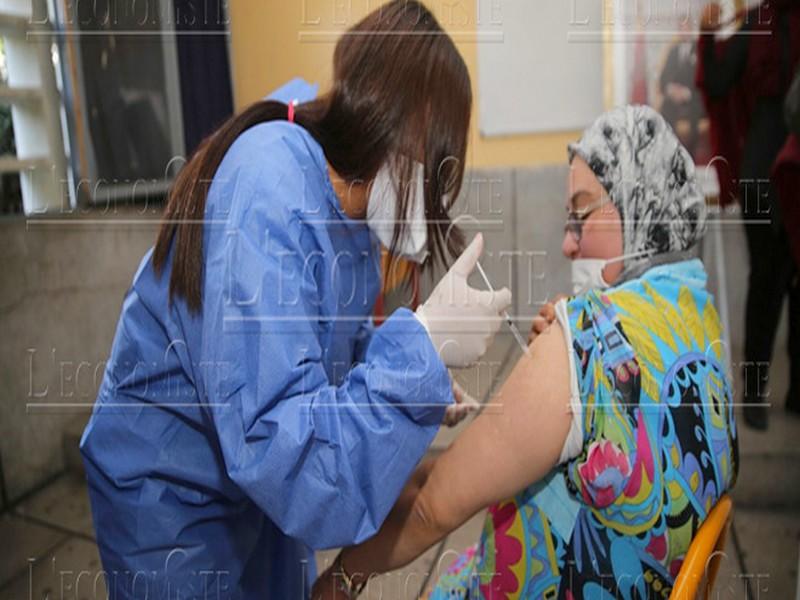
#MAROC_Covid19_3/03/2021: 3,65 millions de personnes vaccinées, 293.857 reçoivent leur 2e dose
Le Maroc a enregistré 393 nouveaux cas de Covid-19 durant les dernières 24 heures, ce qui porte le total à 484 159 cas confirmés, d'après le nouveau bi...
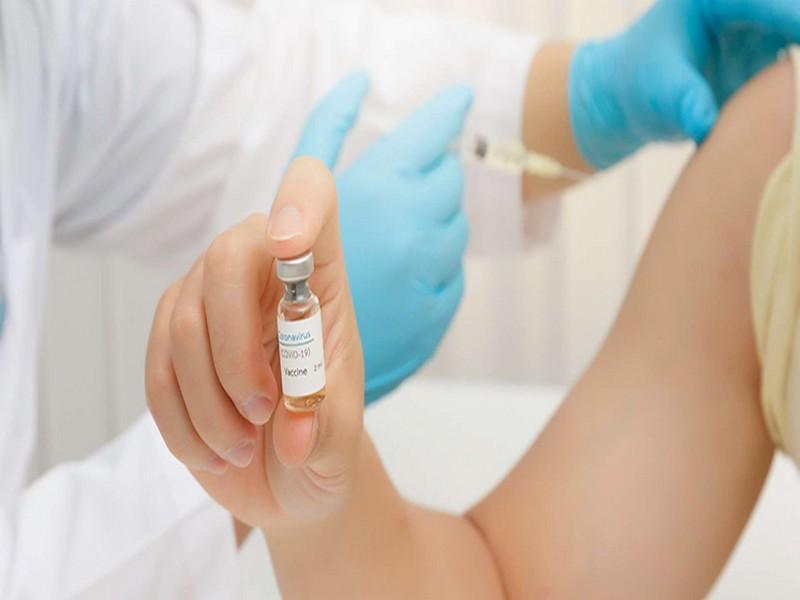
#MAROC_CORONAVIRUS_25_02_2021: Covid-19 au Maroc : 386 nouvelles infections et plus de 3.16 millions
386 nouveaux cas d’infection au coronavirus et 726 guérisons ont été enregistrés au Maroc dans les dernières 24 heures, a annoncé Jeudi le ministère de...


 jeudi 12 novembre 2020
jeudi 12 novembre 2020 0
0 







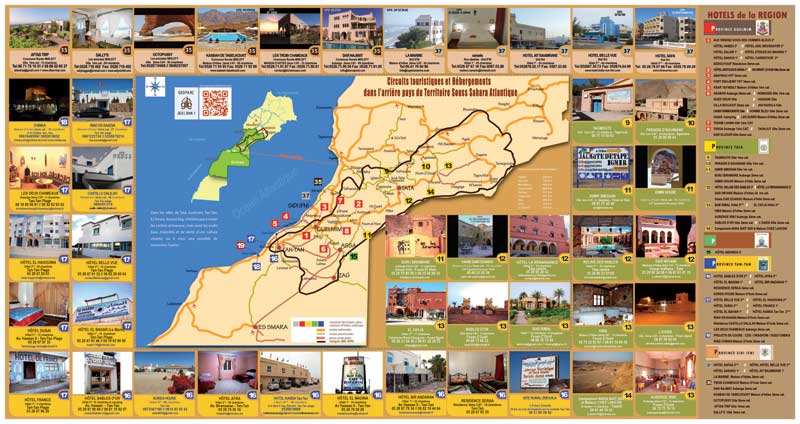
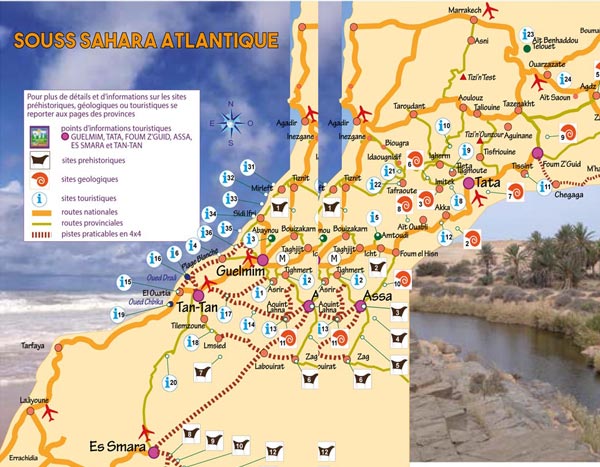
































 Découvrir notre région
Découvrir notre région